体内研究服务
Ba/F3 异种移植模型概览
我们的 Ba/F3 异种移植模型平台 可帮助研究人员:
✔ 在体内评估激酶抑制剂的药效。
✔ 研究激酶突变肿瘤中的耐药机制。
✔ 比较新一代激酶抑制剂与既往代药物的作用效果。
✔ 生成支持 IND 申报的转化研究数据。
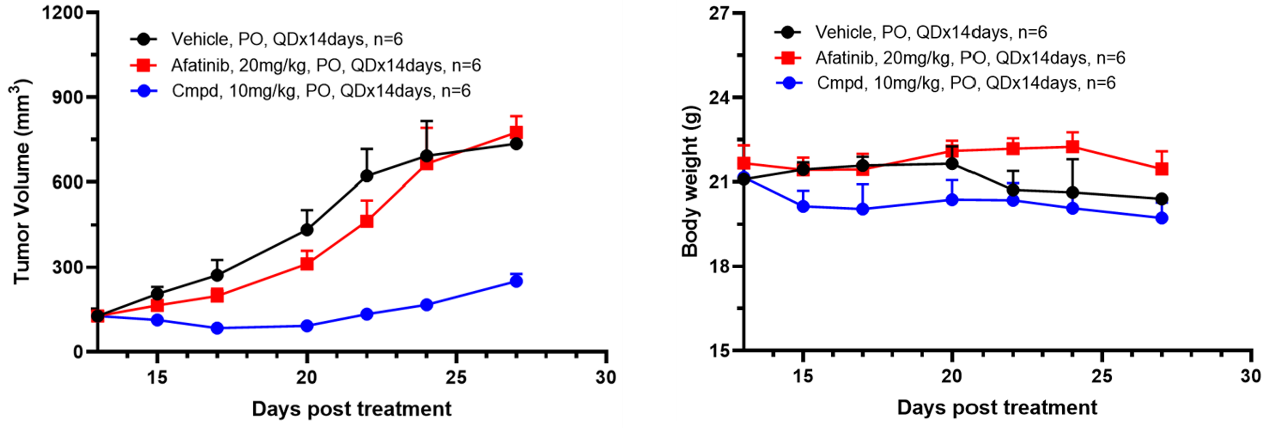
图:皮下 KC-1027-Ba/F3-ERBB2-A775-G776-insYVMA 小鼠模型
蛋白激酶已成为癌症及其他疾病治疗中的重要热门靶点。自 2001 年以来,FDA 已批准超过 70 种激酶抑制剂药物。然而,由于肿瘤存在原发性或获得性耐药,大多数小分子抑制剂只能延缓肿瘤进展。因此,开发具有更高特异性和更低耐药风险的新一代激酶抑制剂仍在持续推进。
Ba/F3 是一种小鼠前 B 细胞系,其生存和增殖依赖于 IL-3。在导入驱动基因后,例如激酶基因或其突变体,Ba/F3 细胞可由 IL-3 依赖转变为驱动基因依赖。基于这一特性,Ba/F3 细胞成为发现新型激酶抑制剂的有力工具。
康源博创团队已构建 700 余株稳定转染激酶基因突变体的 Ba/F3 工程化细胞系。这些 Ba/F3 激酶细胞系均经过测序、Western blot 和抑制剂测试等多维度验证,覆盖多种热门激酶靶点,包括 EGFR(>150 株细胞系)、RAS(80 株细胞系)、FGFR(55 株细胞系)、ERBB2(49 株细胞系)、MET(41 株细胞系)、RET(39 株细胞系)、BCR-ABL(37 株细胞系)、EML4-ALK(33 株细胞系)、FLT3(26 株细胞系)等。大多数经转化的 Ba/F3 细胞系均可用于免疫缺陷小鼠异种移植模型构建。
基于这些 Ba/F3 激酶细胞系来源的异种移植模型,我们建立了体内筛选平台,可用于评估候选药物针对特定激酶突变类型的药效和毒性。同时,我们还可将候选药物与既往代药物进行对比分析。
综上,我们的数据表明,Ba/F3 激酶细胞系来源的异种移植模型是发现新一代激酶抑制剂的重要工具。
Ba/F3 异种移植模型服务流程
我们的 Ba/F3 异种移植筛选平台 采用系统化服务流程,助力生成高质量临床前研究数据:
1️⃣ Ba/F3 细胞系选择
根据治疗靶点,筛选相关激酶突变型 Ba/F3 细胞系。
2️⃣ 肿瘤接种与模型建立
在免疫缺陷小鼠中建立异种移植肿瘤模型。
3️⃣ 激酶抑制剂给药与治疗监测
评估候选药物针对目标突变的体内药效。
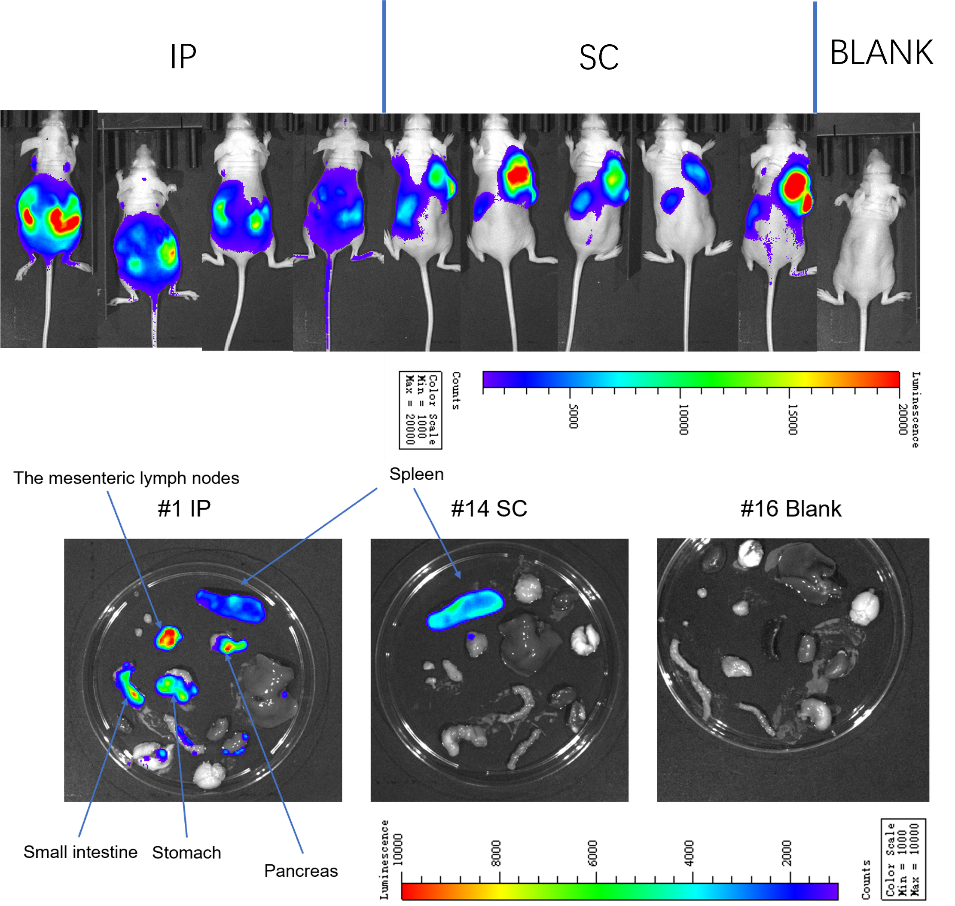
4️⃣ 生物发光与肿瘤生长分析
利用实时成像技术追踪肿瘤响应和生长变化。
5️⃣ 综合数据报告交付
提供深入的数据报告,涵盖剂量-反应关系、毒性评估及耐药机制分析。
每项研究均可根据具体药物开发目标进行定制,以确保实验设计的科学严谨性和转化研究相关性。
Ba/F3 异种移植模型在激酶药物开发中的优势
Ba/F3 异种移植模型为激酶抑制剂评价提供了高度灵活且重复性良好的研究平台。其核心优势包括:
✔ 700+ 工程化 Ba/F3 细胞系 —— 覆盖广泛的激酶基因突变类型。
✔ 经验证的异种移植肿瘤模型 —— 已建立 EGFR、RAS、FGFR、ERBB2、MET、RET、BCR-ABL、ALK、FLT3 等多种靶点相关模型。
✔ 直接评估激酶依赖性 —— 可区分激酶驱动型增殖与 IL-3 依赖型增殖。
✔ 适用于耐药机制研究 —— 支持小分子抑制剂获得性耐药机制的深入探索。
✔ 无缝衔接体外药物筛选 —— 与体外激酶活性检测形成互补,实现体内药效验证。
我们的 Ba/F3 异种移植模型兼具可扩展性与高效性,可帮助客户更快速、更经济地推进临床前药物评价。
激酶抑制剂研究专业支持
我们的 Ba/F3 异种移植模型研究团队可在临床前药物评价的各个阶段提供科学指导与技术支持:
📌 模型选择与研究设计 —— 根据激酶靶点特征定制研究方案。
📌 肿瘤生长与药效响应监测 —— 采用实时生物发光成像技术追踪肿瘤进展与治疗反应。
📌 作用机制与耐药机制研究 —— 深入解析激酶突变驱动的耐药通路。
📌 法规支持与 IND 申报准备 —— 提供支持临床申报的数据包与研究资料。
通过 Ba/F3 异种移植模型,我们助力生物医药研究人员加速激酶靶向药物的开发进程。
Ba/F3 异种移植模型常见问题(FAQs)
所有体内研究服务
Ba/F3 异种移植模型聚焦蛋白激酶这一肿瘤研究中的关键靶点领域。随着激酶类药物在临床治疗中的重要性不断提升,该模型可为肿瘤药物研发提供有价值的体内研究数据,助力研究人员更深入理解激酶驱动型肿瘤的发生发展及药物响应机制。
基因编辑异种移植模型利用 CRISPR/Cas9 等基因编辑工具,对肿瘤细胞基因组进行精准修饰,从而构建更具靶点特异性和疾病相关性的肿瘤模型。该技术显著拓展了现代肿瘤学研究的方法边界与应用潜力,为肿瘤发生机制、靶点功能验证及药物疗效评价提供更深入的研究依据。
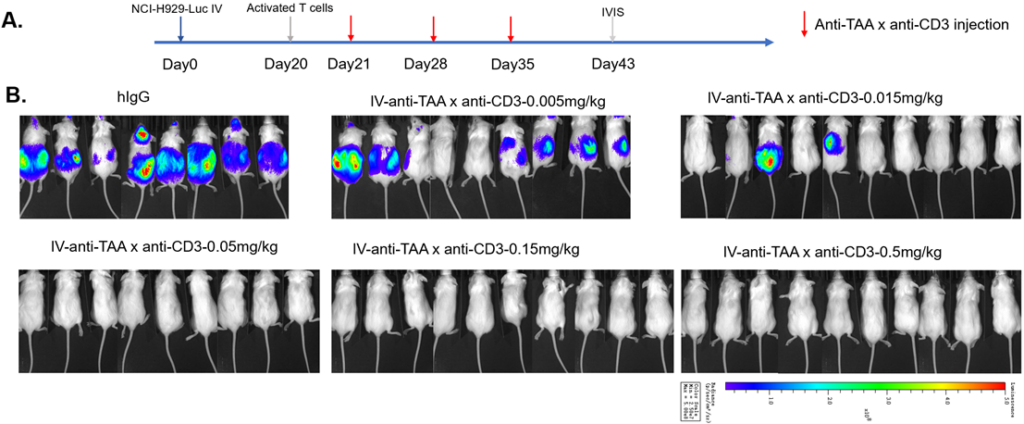
荧光素酶标记肿瘤模型可用于研究肿瘤生长过程及免疫微环境动态变化。借助生物发光成像技术,该模型能够实现对肿瘤进展的实时、动态监测。该创新性研究方法有助于加深对肿瘤发生发展机制的理解,推动癌症研究进展,并促进新型治疗策略的发现与开发。
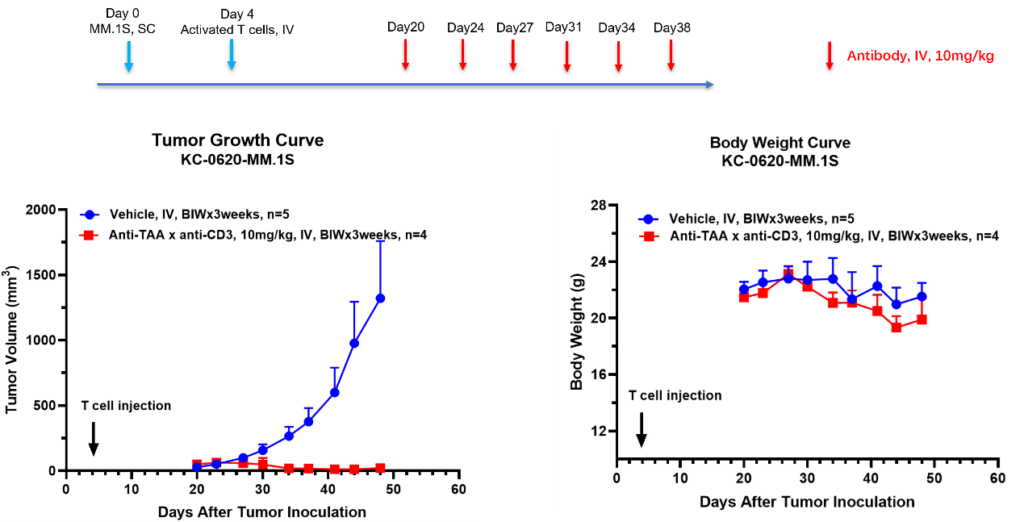
PBMC 人源化小鼠模型能够在体内重建并模拟人源 T 细胞的行为特征,为肿瘤免疫学研究提供精细化分析平台。该模型为深入探索肿瘤免疫反应、免疫细胞功能及免疫治疗机制提供了独特路径,有助于丰富临床前研究数据,并构建更加全面的人源化体内药效评价体系。
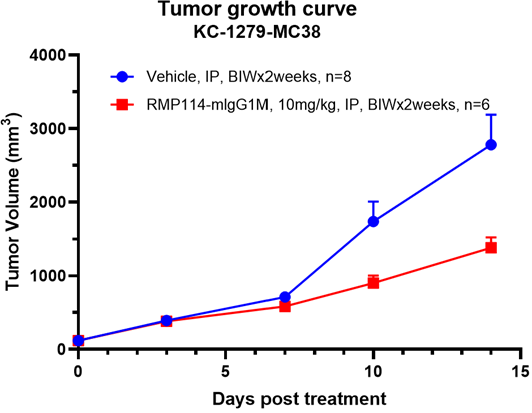
同系移植模型采用来源于小鼠的肿瘤组织或肿瘤细胞,并将其接种至遗传背景相同或相近的宿主体内,有助于提升肿瘤研究的一致性和研究深度。该模型能够在免疫功能完整的体内环境中开展癌症研究,为肿瘤免疫、药效评价及联合治疗研究提供更贴近真实生理状态的实验平台。
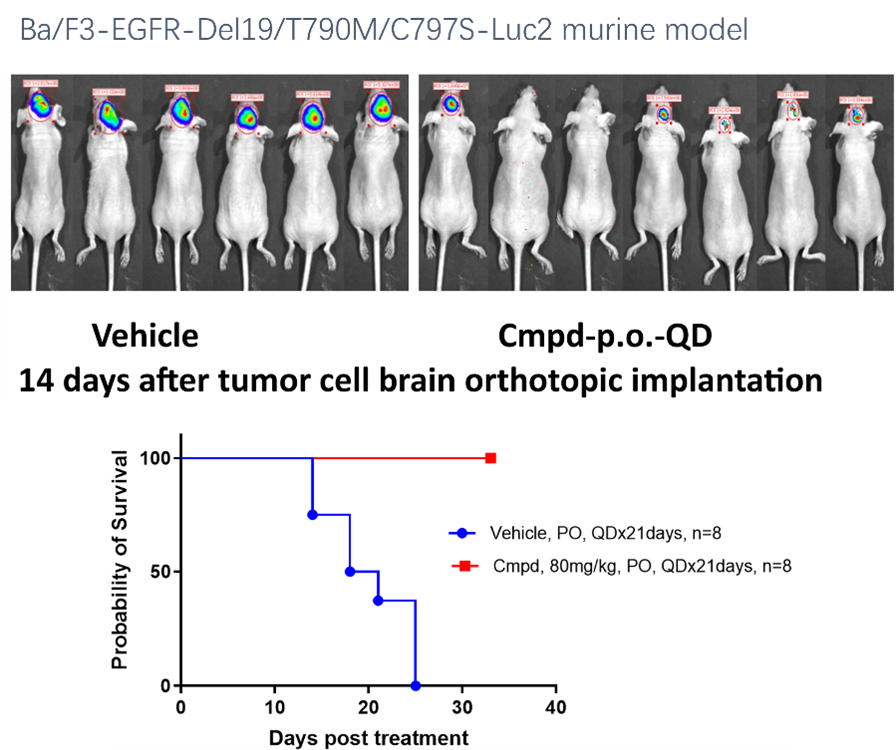
原位肿瘤模型是评估抗肿瘤药物疗效、支持临床转化研究及探索潜在治疗策略的重要模型选择。该模型通过将肿瘤细胞或组织接种于其对应的原发解剖部位,更好地模拟肿瘤在体内的生长环境、组织微环境及转移特征。作为肿瘤治疗研究中的成熟模型体系,原位肿瘤模型可为药效评价、机制研究和临床前开发提供更具转化价值的数据支持。