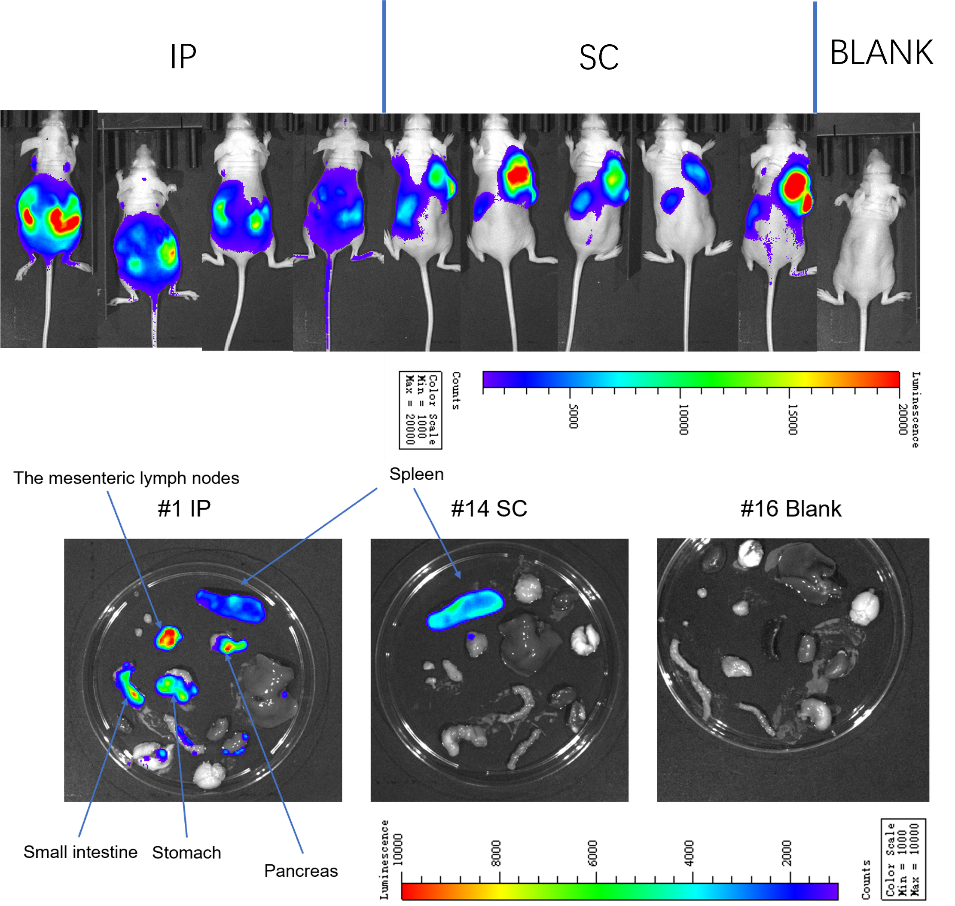
荧光素酶标记肿瘤模型
体内研究服务
荧光素酶标记肿瘤模型概览
荧光素酶标记肿瘤模型是用于研究肿瘤生长与免疫反应的动物模型,也是我们 体内生物学服务的重要技术平台。在该模型中,肿瘤细胞经荧光素酶基因标记后可产生生物发光信号,研究人员可在活体动物中动态监测肿瘤生长、转移和播散。
目前,康源博创已构建 50 种携带 Luciferase 标记的肿瘤细胞系,并基于这些细胞建立了系统性模型、皮下模型、脑原位模型、肿瘤转移模型等多种模型体系。
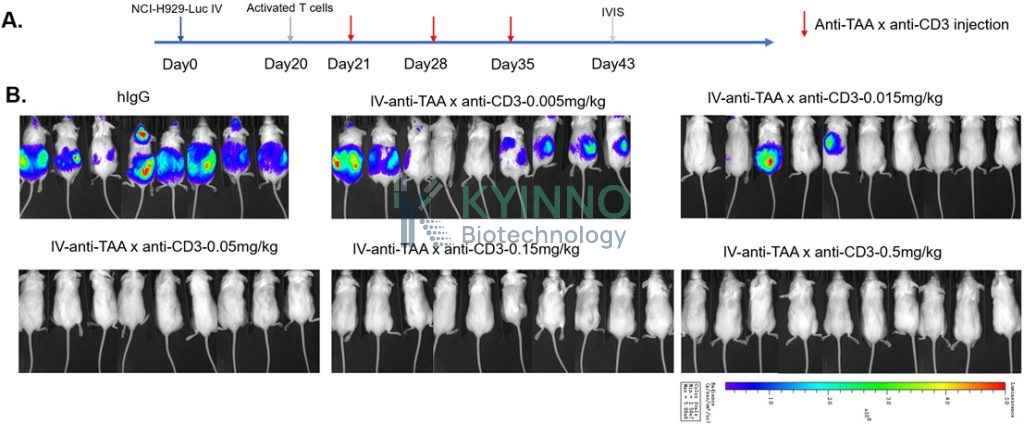
基于荧光素酶模型的体内研究流程
我们的荧光素酶肿瘤模型研究采用简洁、可重复的流程,兼顾方案灵活性与数据完整性:
肿瘤细胞系选择与荧光素酶标记
我们可提供覆盖主要癌种的荧光素酶表达肿瘤细胞系,也可根据需求为客户提供的细胞系导入荧光素酶报告基因。
模型建立
根据研究目标,将肿瘤细胞通过原位移植、皮下接种或转移模型方案接种至免疫缺陷小鼠。
成像方案实施
采用高灵敏度平台进行生物发光成像。成像频率可根据给药方案或肿瘤进展速度进行调整。
数据采集与肿瘤监测
纵向记录发光信号强度,为肿瘤体积和位置提供定量读出。来自活细胞的信号输出使研究人员可在无需终末处置动物的情况下评估细胞活性。
数据分析与报告
对肿瘤生长动力学和治疗疗效进行统计分析,并根据客户需求交付定制化报告和原始数据。
技术规格与定制化选项
- 肿瘤接种部位(如脑、侧腹、肺)
- 治疗起始时间
- 与人源免疫细胞共同移植
- 兼容的附加检测(如 IHC、流式细胞术)
- 可选分析包括蛋白-蛋白相互作用、基因转移和研究后细胞克隆等。
| 参数 | 详情 |
|---|---|
| 物种 | 免疫缺陷小鼠 |
| 成像系统 | 生物发光 IVIS |
| 定制化 | 肿瘤部位、共同移植等 |
| 可用细胞系 | 覆盖多癌种的 50 余种细胞系 |
荧光素酶肿瘤模型在癌症研究中的优势
荧光素酶肿瘤模型具有多项实验优势,是临床前癌症研究和治疗药物开发中价值较高的工具。
- 在活体动物中实时可视化肿瘤
- 定量、非侵入性追踪肿瘤负荷
- 通过纵向数据采集减少动物使用
- 对早期肿瘤反应具有较高检测灵敏度
- 适用于肿瘤学、免疫肿瘤学和基因治疗评价
- 支持皮下、原位和转移性肿瘤研究
- 支持分子影像学应用,灵敏度高于传统光学方法
荧光素酶模型在临床前研究中的应用
荧光素酶模型可用于广泛的肿瘤学研究应用:
- 小分子、生物制剂或免疫疗法的临床前药物筛选
- 肿瘤-宿主相互作用和免疫细胞浸润分析
- 转移模型构建,可追踪肿瘤向淋巴结等继发部位的播散
- 尤其适用于追踪肿瘤结节、脑转移和局部浸润
- 基因编辑条件下的肿瘤生长分析,包括基因敲除或过表达研究
开启荧光素酶肿瘤模型研究
荧光素酶肿瘤模型是一个灵活且数据丰富的平台,适合推进转化肿瘤研究。我们的团队将根据您的治疗开发或机制研究目标,协助设计定制化研究方案。
预约免费咨询,沟通模型选择、定制化选项或研究可行性。
荧光素酶肿瘤模型常见问题
1. 与其他分子影像技术相比,生物发光成像如何提升肿瘤追踪?
2. 可提供哪些携带荧光素酶报告基因的癌症细胞系?
3. 体内生物发光成像系统的检测灵敏度如何?
我们的成像平台可根据组织深度和荧光素酶活性检测低至约 10⁴ 个细胞的生物发光信号。该灵敏度支持肿瘤早期检出和纵向监测,无需在每个时间点处死动物。
4. 荧光素酶模型能否用于评价免疫反应或肿瘤微环境?
5. 荧光素酶表达模型是否兼容基因表达谱、IHC 等检测?
6. 如何在活细胞动物模型中定量荧光素酶活性?
7. 用于体内成像时,荧光素酶与荧光蛋白有什么区别?
8. 荧光素酶成像能否用于异种移植模型的基因表达研究?
9. 什么是体内生物发光成像,它如何应用于肿瘤研究?
10. 荧光素酶报告细胞系能否用于小鼠模型中的转移追踪?
所有体内研究服务
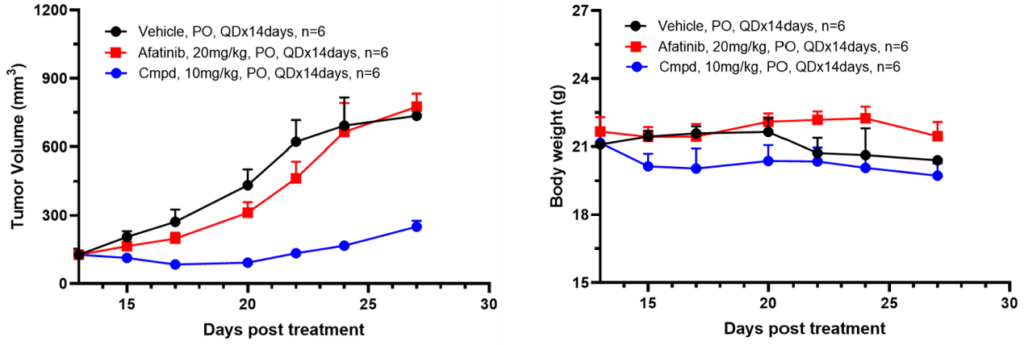
Ba/F3 异种移植模型聚焦蛋白激酶这一肿瘤研究中的关键靶点领域。随着激酶类药物在临床治疗中的重要性不断提升,该模型可为肿瘤药物研发提供有价值的体内研究数据,助力研究人员更深入理解激酶驱动型肿瘤的发生发展及药物响应机制。
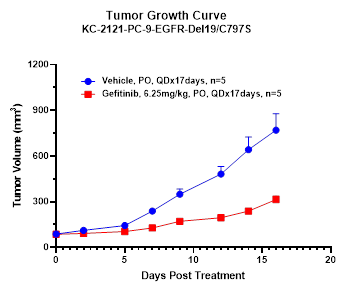
基因编辑异种移植模型利用 CRISPR/Cas9 等基因编辑工具,对肿瘤细胞基因组进行精准修饰,从而构建更具靶点特异性和疾病相关性的肿瘤模型。该技术显著拓展了现代肿瘤学研究的方法边界与应用潜力,为肿瘤发生机制、靶点功能验证及药物疗效评价提供更深入的研究依据。
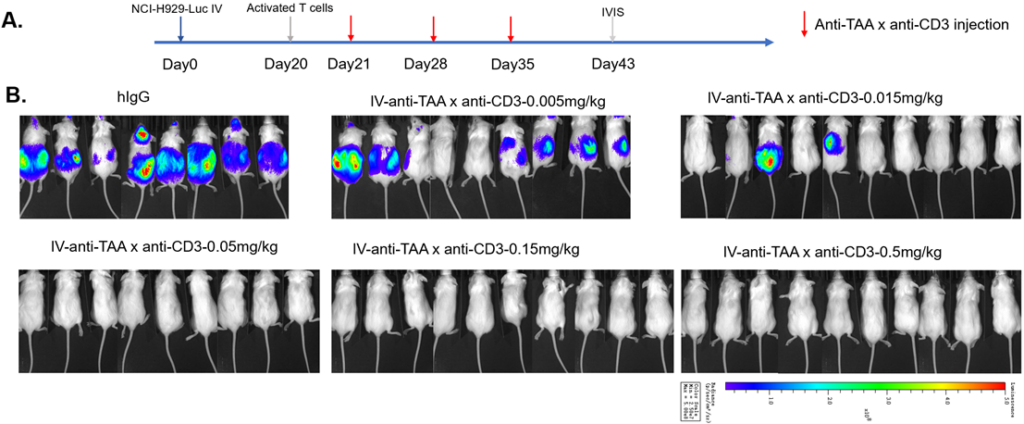
荧光素酶标记肿瘤模型可用于研究肿瘤生长过程及免疫微环境动态变化。借助生物发光成像技术,该模型能够实现对肿瘤进展的实时、动态监测。该创新性研究方法有助于加深对肿瘤发生发展机制的理解,推动癌症研究进展,并促进新型治疗策略的发现与开发。
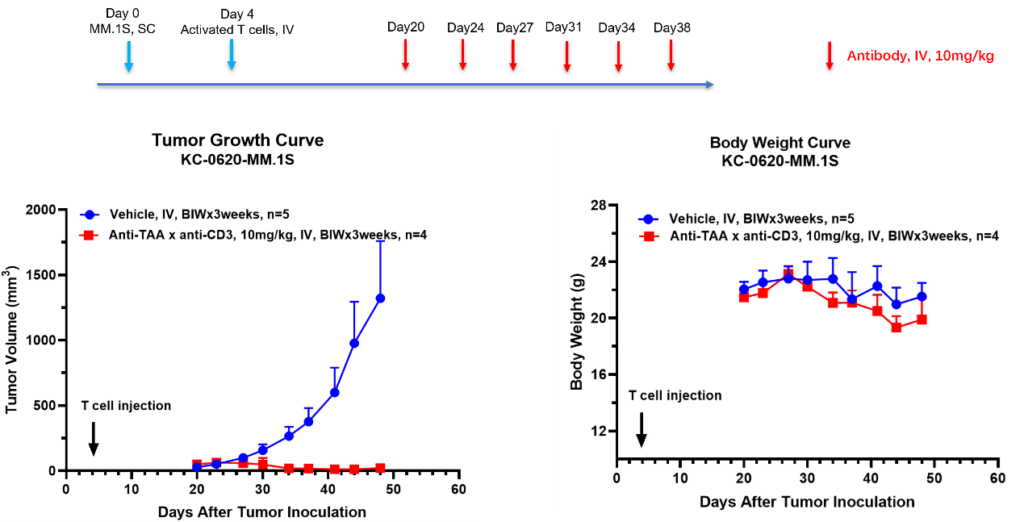
PBMC 人源化小鼠模型能够在体内重建并模拟人源 T 细胞的行为特征,为肿瘤免疫学研究提供精细化分析平台。该模型为深入探索肿瘤免疫反应、免疫细胞功能及免疫治疗机制提供了独特路径,有助于丰富临床前研究数据,并构建更加全面的人源化体内药效评价体系。
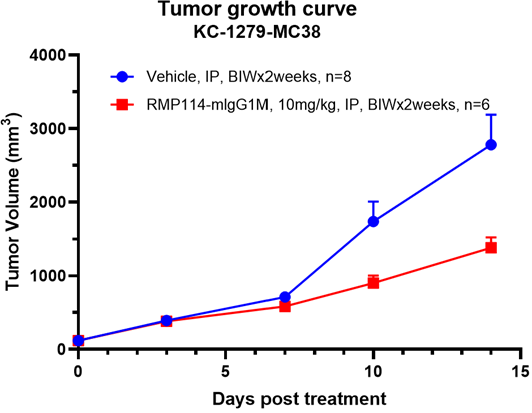
同系移植模型采用来源于小鼠的肿瘤组织或肿瘤细胞,并将其接种至遗传背景相同或相近的宿主体内,有助于提升肿瘤研究的一致性和研究深度。该模型能够在免疫功能完整的体内环境中开展癌症研究,为肿瘤免疫、药效评价及联合治疗研究提供更贴近真实生理状态的实验平台。
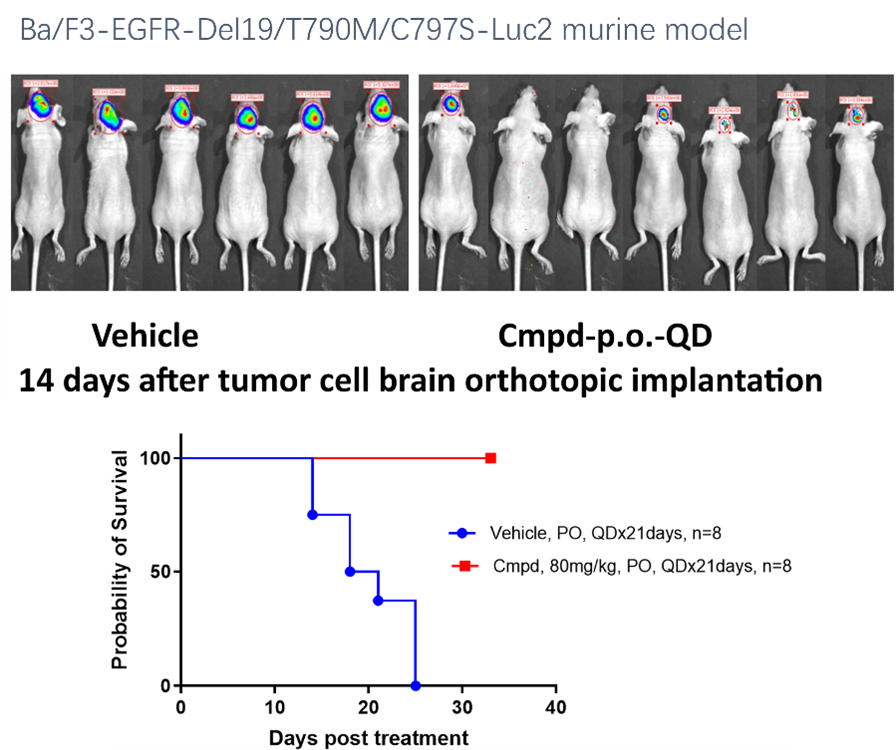
原位肿瘤模型是评估抗肿瘤药物疗效、支持临床转化研究及探索潜在治疗策略的重要模型选择。该模型通过将肿瘤细胞或组织接种于其对应的原发解剖部位,更好地模拟肿瘤在体内的生长环境、组织微环境及转移特征。作为肿瘤治疗研究中的成熟模型体系,原位肿瘤模型可为药效评价、机制研究和临床前开发提供更具转化价值的数据支持。