抗体内吞实验
体外研究服务
细胞内吞实验概述

单克隆抗体目前已广泛应用于癌症、炎症性疾病及抗病毒治疗等领域。抗体进入细胞的程度、位置和速度,是评价抗体药物功能特征的重要指标之一。
治疗性抗体通常被设计用于靶向肿瘤细胞表面的特定受体,从而实现药物载荷的精准递送。抗体偶联药物(ADC)由具有生物活性的细胞毒性小分子药物与单克隆抗体通过化学连接子偶联而成。单克隆抗体作为载体,可将小分子药物递送至目标细胞。
当抗体与细胞表面抗原结合后,抗体的内吞过程可使小分子药物进入靶细胞,并发挥细胞毒作用。因此,抗体内吞能力是 ADC 药物早期筛选中的关键评价指标。
康源博创的抗体内吞实验是体外研究服务的重要组成部分,可通过精准的细胞功能检测方法,支持靶向治疗药物的开发与评价。
内吞作用在 ADC 开发中的重要性
内吞作用决定了 ADC 是否能够高效地将药物载荷递送至靶细胞。具有快速且特异性摄取能力的抗体通常可提升 ADC 药效,同时降低脱靶毒性。相反,内吞能力较低或摄取不均一的抗体,可能降低治疗效果并增加全身暴露风险。
由于不同抗体-抗原组合及肿瘤类型之间的内吞速率存在差异,因此在相关细胞模型中测定摄取动力学至关重要。例如,使用 HT1080 细胞 等模型可帮助筛选更具开发潜力的 ADC 候选药物,并优化连接子和载荷设计策略,从而提升 ADC 药效并支持靶向治疗药物开发。
内吞检测平台与技术
康源博创支持多种检测形式,以满足 ADC 研究中的不同需求:
- Fab-zap 内吞试剂盒 —— 利用毒素偶联的 Fab 片段,定量评估抗体介导的细胞摄取及其功能性递送能力。
- pHrodo 荧光检测系统 —— 采用 pHrodo 染料进行荧光成像,该染料在受体介导的内吞过程中进入酸性内体区室后信号增强。
- αHFc-CL-MMAF 内吞检测体系 —— 利用偶联细胞毒素评估抗体摄取及载荷实时释放情况。
- 靶点剥离法 —— 区分细胞表面结合抗体与已内吞抗体,准确评估摄取动力学,并提供受体内吞相关机制信息。
所有平台均兼容高通量实验流程,包括 384 孔板 及其他检测板设置,可实现多个抗体样品的并行筛选。检测读数包括荧光信号追踪、内吞速率曲线和定量摄取图谱,为研究人员提供可重复、可用于决策的数据支持。
为什么选择康源博创的内吞实验服务?
康源博创将先进的检测技术与肿瘤学和炎症研究领域的专业经验相结合。我们的服务旨在:
- 通过经过验证的高通量实验方案提供可靠结果。
- 借助多种检测平台支持不同研究需求。
- 提供从检测方案选择到数据解读的全流程项目支持。
- 与 Kyinno 更广泛的抗体发现和下游功能检测服务无缝整合。
这种端到端服务模式可为抗体偶联药物(ADC)候选分子的筛选提供可靠数据支持,帮助客户更有信心地推进候选药物选择。
交付内容与报告形式
每项研究包括:
- 内吞曲线和荧光信号数据集。
- 不同抗体之间摄取速率的定量比较。
- 包含实验验证说明的详细方法学信息。
- 可选整合结合实验、降解实验或下游药效研究。
治疗性抗体与 ADC 研究中的应用
康源博创的内吞实验服务可支持治疗药物开发的多个阶段:
- 早期 ADC 筛选,用于识别具有强受体内吞能力的抗体。
- 单克隆抗体偶联前验证。
- 比较不同靶点、肿瘤类型或工程化抗体形式的内吞动力学。
- 生成支持 ADC 设计的数据,包括连接子化学和载荷选择策略,以帮助降低肿瘤生长。
开启内吞实验生物学服务
康源博创的内吞实验服务可支持治疗药物开发的多个阶段:
- 早期 ADC 筛选,用于识别具有强受体内吞能力的抗体。
- 单克隆抗体偶联前验证。
- 比较不同靶点、肿瘤类型或工程化抗体形式的内吞动力学。
- 生成支持 ADC 设计的数据,包括连接子化学和载荷选择策略,以帮助降低肿瘤生长。
立即预约免费咨询,讨论您的项目需求。
内吞实验常见问题(FAQs)
1. 什么是抗体内吞实验?为什么它在药物开发中很重要?
抗体内吞实验用于评估抗体与细胞表面抗原结合后,通过受体介导的内吞作用进入肿瘤细胞的效率。该过程对于评估抗体偶联药物(ADC)的有效性至关重要,因为成功的内吞可确保药物载荷被递送至靶细胞,从而提升 ADC 在癌症治疗中的药效。
2. 内吞实验如何应用于治疗性抗体研究?
内吞实验在治疗性抗体和单克隆抗体开发中发挥关键作用。通过评估相关细胞系(如 HT1080 细胞)中的受体内吞速率和抗体摄取情况,研究人员可以识别具有较强细胞表面受体结合能力的抗体,并优化其作为靶向治疗药物的开发潜力。
3. 常用于追踪肿瘤细胞中抗体内吞的方法有哪些?
抗体内吞可通过多种方法进行监测,包括流式细胞术、荧光染料成像、pH 敏感染料检测,以及基于 pHrodo 染料的先进检测平台。这些技术可帮助研究人员定量分析摄取动力学、可视化内吞路径,并区分细胞表面结合抗体与已内吞抗体。
4. 抗体偶联药物如何依赖抗体内吞?
抗体偶联药物依赖高效的抗体内吞,将细胞毒性药物载荷递送至靶向肿瘤细胞。当抗体与细胞表面受体结合后,会发生受体介导的内吞,将药物带入内体区室中。这一过程有助于实现靶向递送,降低脱靶效应,并增强抗体偶联药物的治疗获益。
5. 在抗体发现中使用抗体内吞实验有哪些优势?
在抗体发现阶段,早期评估抗原表达和细胞表面表达有助于识别最具开发潜力的抗体偶联药物候选分子。借助 384 孔板筛选等高通量细胞检测平台,研究人员可以快速评估内吞动力学、通过二抗验证结合情况,并生成可靠数据,从而加速具有治疗潜力抗体的开发。
全部体外研究服务
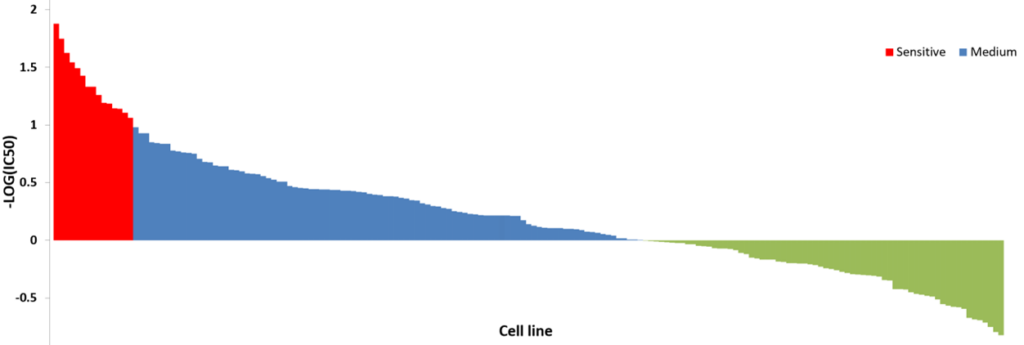
通过深入了解驱动肿瘤细胞表型的遗传异常,可显著提升肿瘤细胞系作为研究模型和药物发现工具的应用价值。Kyinno 的 MegaScreen 细胞面板筛选服务可为药物发现和生物标志物开发项目提供定制化研究支持。

类器官是在体外培养形成的复杂 3D 器官模拟模型,在生物医学研究中具有重要价值,可用于疾病建模、药物测试以及器官发育研究。康源博创擅长从多种肿瘤组织中培养类器官,并与肿瘤专科医院紧密合作,确保研究模型具有良好的转化相关性。