肿瘤相关抗原(TAA)同系模型
体内药理服务平台
TAA 同系模型概述
肿瘤相关抗原(Tumor-associated Antigens, TAA)是在肿瘤细胞上特异性表达或高表达,而在正常组织中不表达或低表达的抗原分子。这些分子在肿瘤增殖、分化及转移过程中发挥关键作用,使其成为抗肿瘤药物研发的核心治疗靶点。
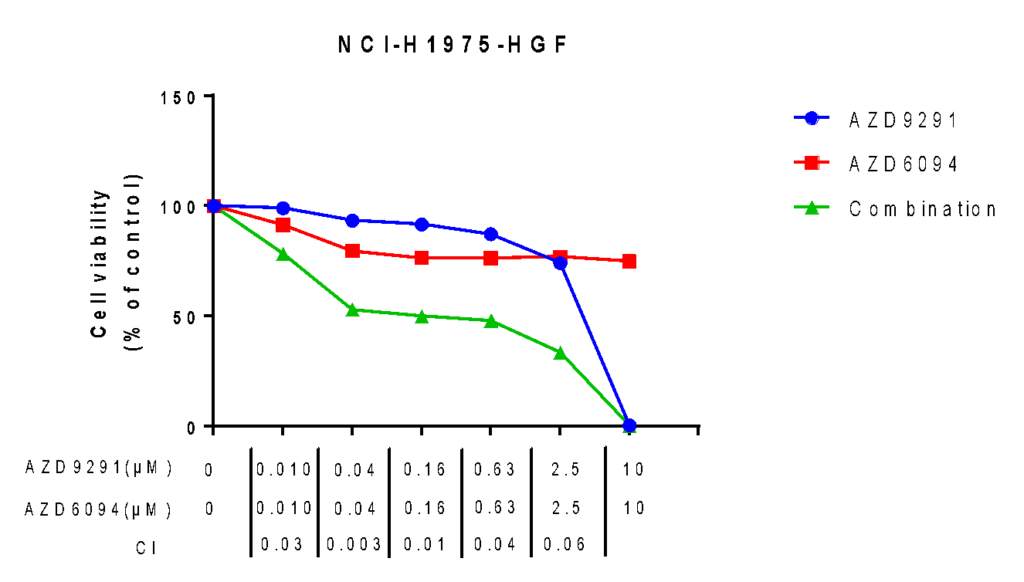
针对肿瘤相关抗原(TAA)的药物可通过抗体依赖的细胞介导的细胞毒性作用(ADCC)、补体依赖的细胞毒性作用(CDC)以及激活免疫应答,诱导肿瘤细胞杀伤。
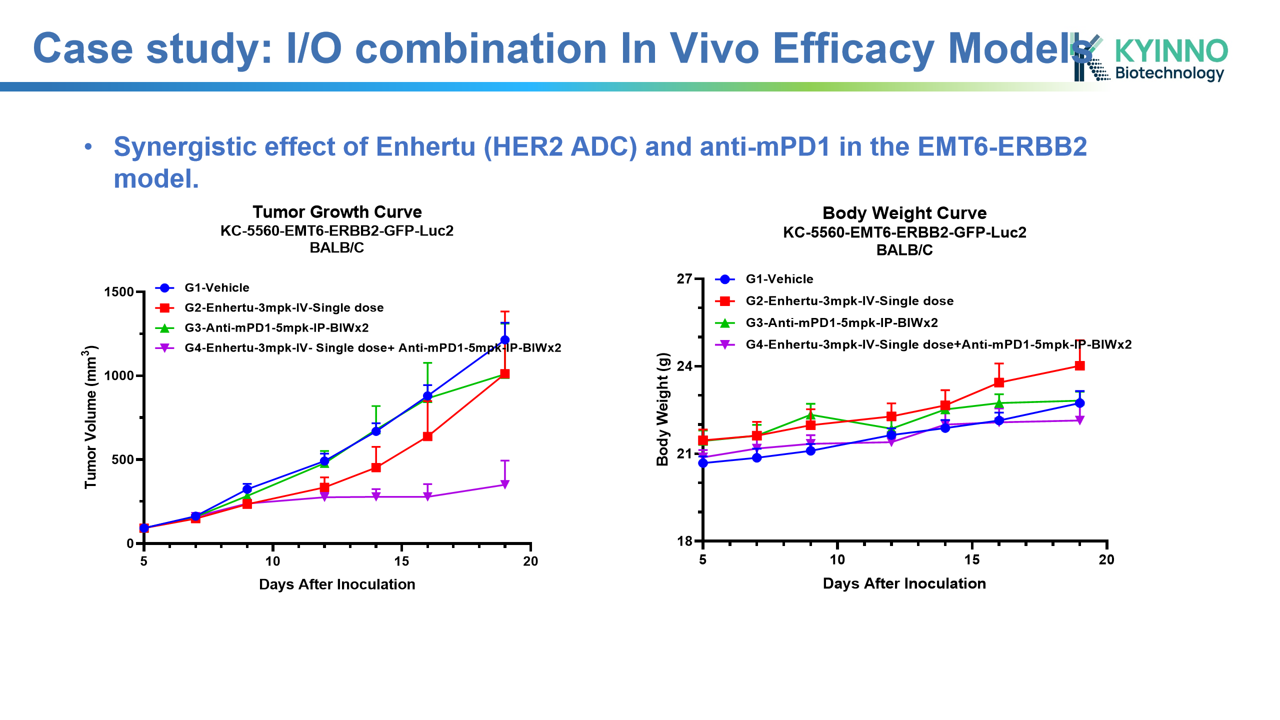
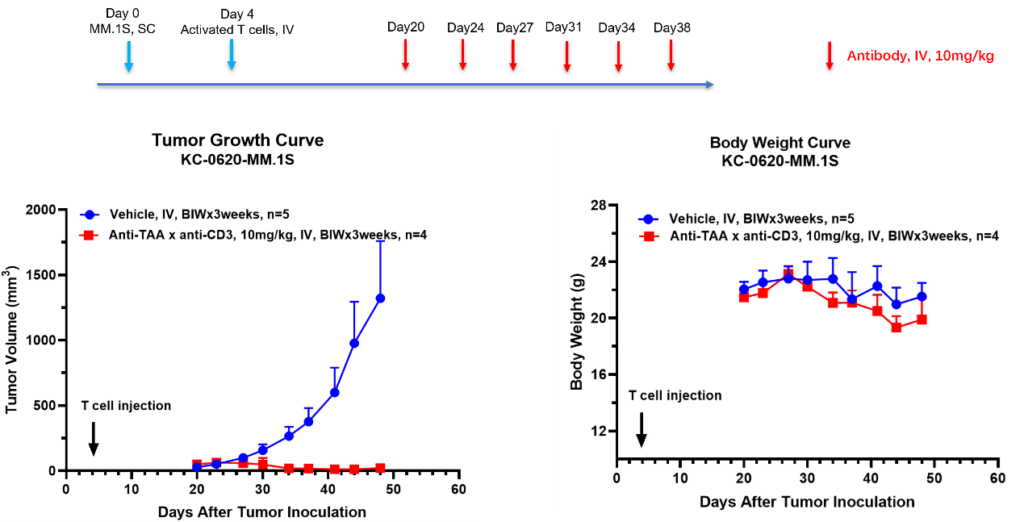
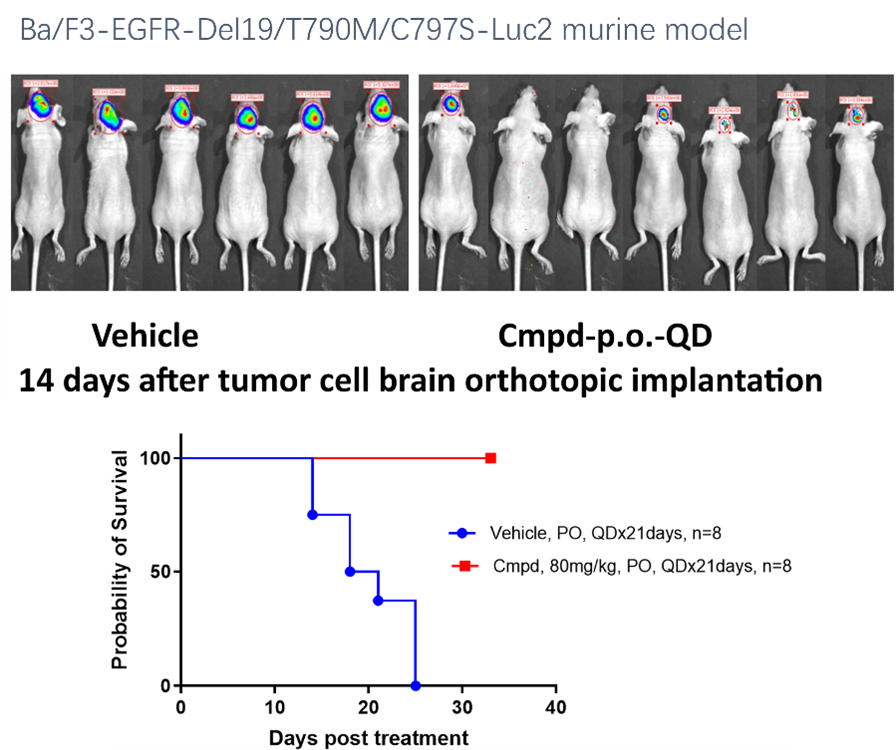
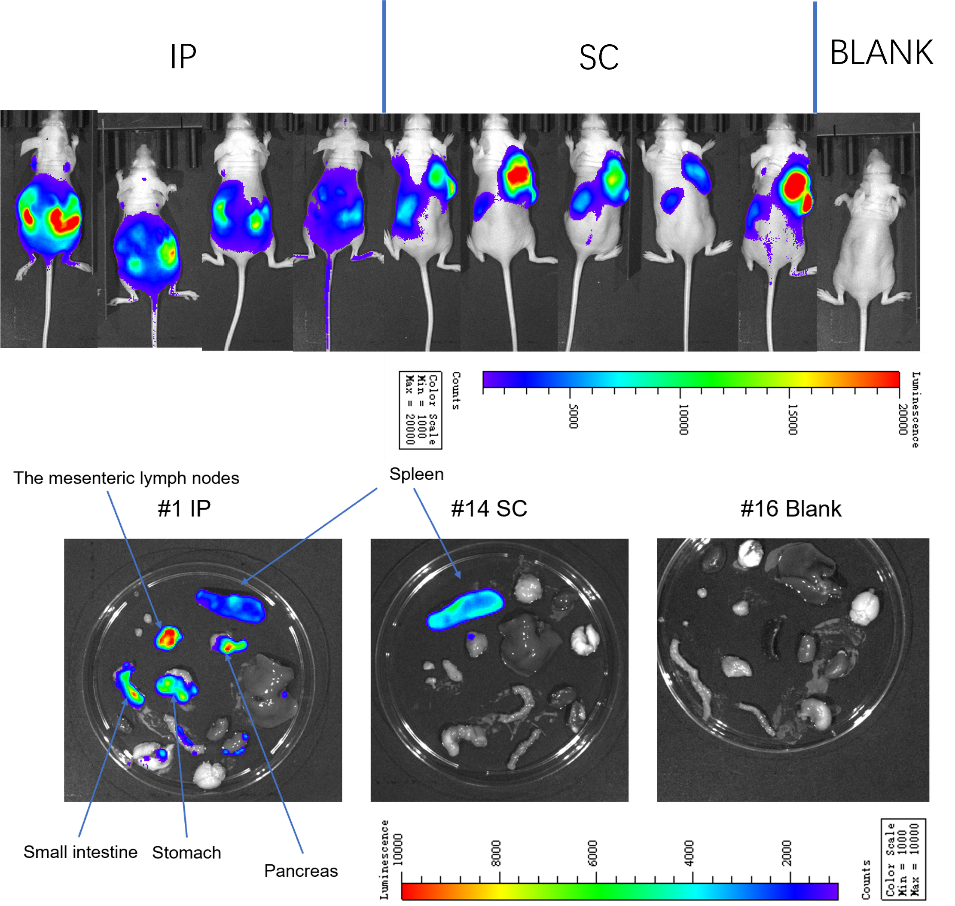
为支持此类治疗药物的体内药效学测试,康源博创已建立一套全面的肿瘤相关抗原(TAA)人源化细胞系。当这些人源化肿瘤细胞被皮下或原位接种到相同遗传背景的野生型小鼠体内时,会构建出同源小鼠模型。该模型可保留免疫系统完整性,助力在免疫健全的环境中精准评估药物疗效。
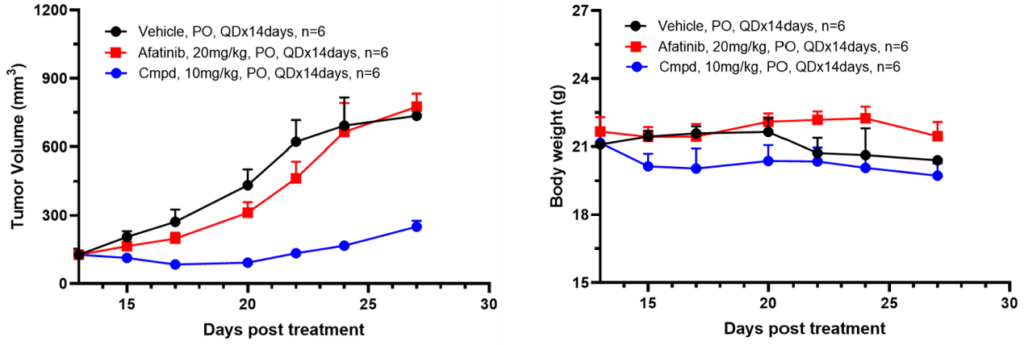
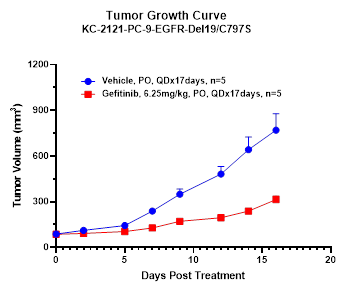
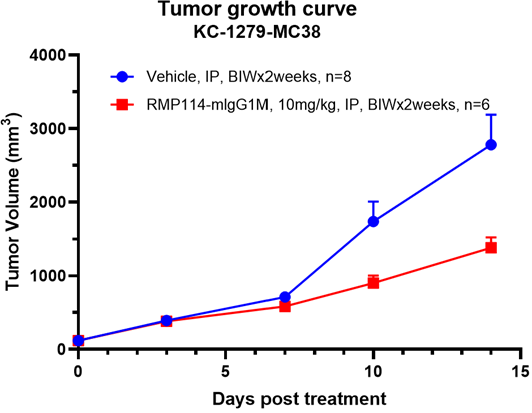
TAA 靶向药物体内药效评价
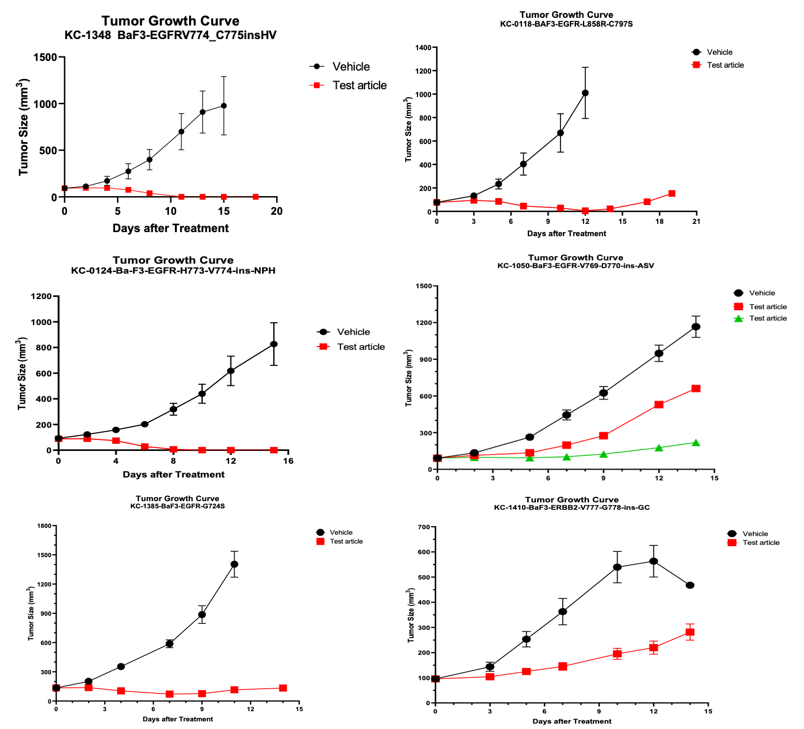
肿瘤相关抗原(TAA)在肿瘤细胞中高表达或特异表达,是抗肿瘤药物开发的关键靶点。针对 TAA 的药物可通过 ADCC、CDC 及激活免疫反应诱导肿瘤细胞死亡。
TAA 人源化细胞系资源
康源博创构建了超 500 株 TAA 人源化细胞系,可在免疫健全的小鼠模型中准确评估药物效果。
模型优势
该模型保留完整免疫系统,适用于抗体药物、TAA 靶向药物、免疫治疗及联合疗法的体内疗效评价。
应用场景
可用于候选药物体内药效评价、TAA 靶点验证、ADCC/CDC 作用机制研究和免疫相关疗效分析。
开启 TAA 同系模型研究
欢迎联系我们,根据您的 TAA 靶点和药物类型选择合适的人源化细胞系和同系模型方案。
TAA 同系模型服务咨询
如需启动项目,请提供 TAA 靶点、药物类型、预期作用机制及候选模型需求,我们将协助设计体内药效研究方案。