Ba/F3 激酶细胞系
康源博创 Ba/F3 激酶筛选细胞系
激酶几乎调控细胞活动的各个方面,其表达变化或基因突变可能导致肿瘤和其他疾病的发生发展。二十一年前,首个激酶抑制剂伊马替尼获 FDA 批准,开启了以激酶为靶点的药物开发浪潮。迄今,该领域已有 70 余款新药获批 [1]。然而,这一历程始终伴随希望与失望的循环:药物起初显示临床疗效,但随后出现耐药,导致疾病复发。因此,围绕激酶的开发策略不断演进,包括靶向不同激酶的联合治疗、激酶抑制剂与传统化疗药物联用、靶向激酶的抗体药物、抗体偶联药物、不可逆激酶结合剂、变构激酶结合剂以及利用 AI 进行药物设计等。
截至目前,在 518 个激酶中,仅略多于 50 个成为药物靶点;预计未来 20 年,激酶抑制剂仍将是药物开发的主要增长方向之一 [1]。下一代抑制剂将更强调提高特异性、降低耐药性以及穿透血脑屏障的能力。在耐药问题上,激酶抑制剂与其他治疗模式联合以共同克服耐药,仍将是持续关注的重点。
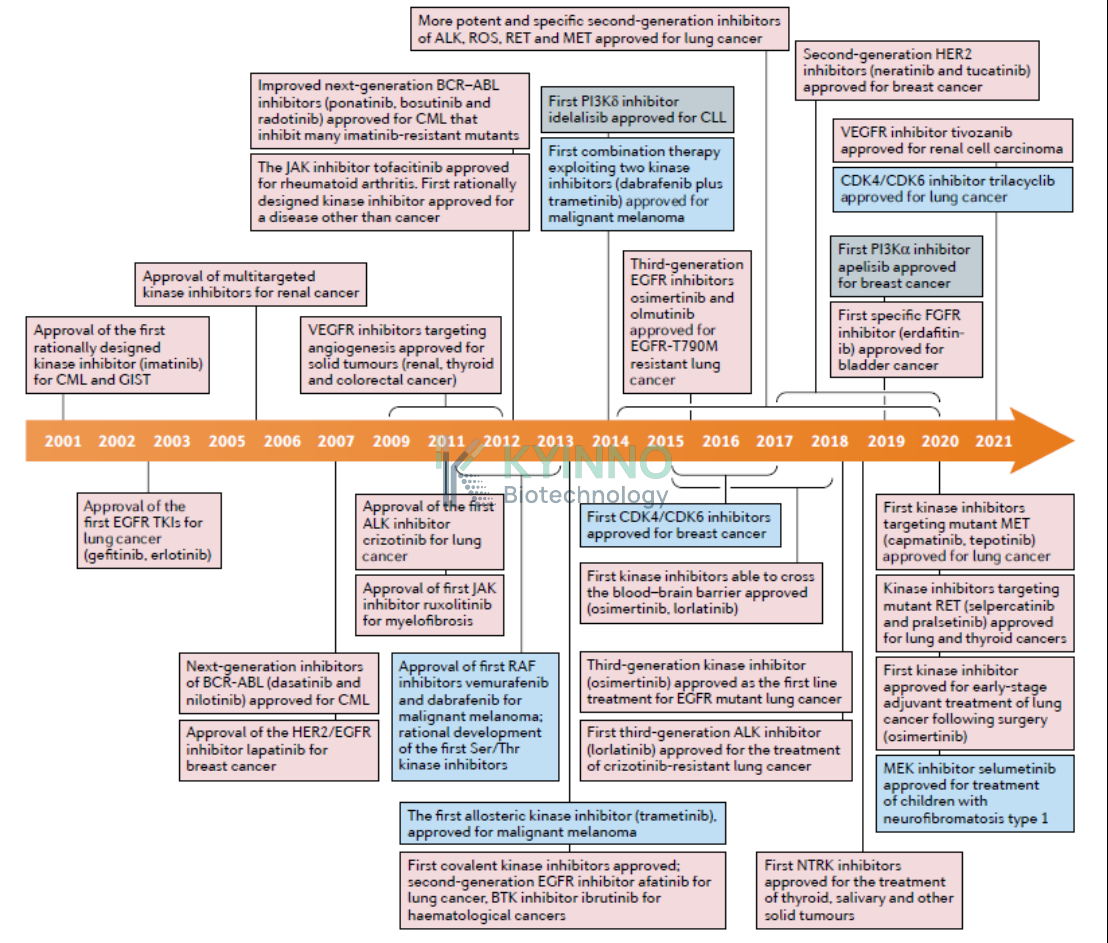
图:自伊马替尼获批以来 20 年间激酶抑制剂药物开发与审批的重要事件。
Ba/F3 激酶筛选细胞系
Ba/F3 细胞是依赖 IL-3 生长的小鼠前 B 细胞。Palacios 和 Steinmetz 于 1985 年首次描述了该细胞系,他们旨在从 Balb/c 小鼠骨髓中分离依赖 IL-3 生长的 pro-B 细胞。随后,Daley 和 Baltimore 证明,逆转录病毒驱动的 Bcr-Abl 酪氨酸激酶表达可使 Ba/F3 细胞脱离 IL-3 而独立生长,由此开启了 Ba/F3 细胞作为肿瘤研究工具,尤其是激酶研究工具的应用。
使 Ba/F3 细胞表达具有组成型活性的激酶,并在无 IL-3 条件下监测细胞生长,为评估激酶转化能力提供了便捷方法 [4]。表达突变激酶的 Ba/F3 细胞可用于评估这些突变如何改变激酶转化能力。由于 Ba/F3 细胞生长迅速,倍增时间约为 20 小时,因此适用于小分子激酶抑制剂的高通量筛选。在这一体系中,Ba/F3 细胞提供单一激酶背景,不受其他激酶干扰,因而具有较高特异性。此外,可利用携带不同突变激酶基因的逆转录病毒感染 Ba/F3 细胞 [5],或使用 ENU 诱导表达特定激酶的 Ba/F3 细胞产生突变 [6],用于筛选激酶抑制剂耐药突变。
Ba/F3 细胞在激酶研究和药物发现中的应用基于以下特点:
- 在悬浮培养中生长迅速;
- 易于通过电转染或常用逆转录病毒/慢病毒表达系统进行基因导入;
- 表达具有组成型活性的激酶或其他癌蛋白后,可脱离 IL-3 依赖而独立增殖和存活。
基于 Ba/F3 细胞系,Kyinno 建立了覆盖细胞水平和动物水平的激酶活性筛选平台。目前,我们已构建 8,800 余株 Ba/F3 激酶稳定细胞系,另有 1,100 余株细胞系正在构建中。Kyinno 已为全球 200 余位用户提供药理学和药效学研究服务。
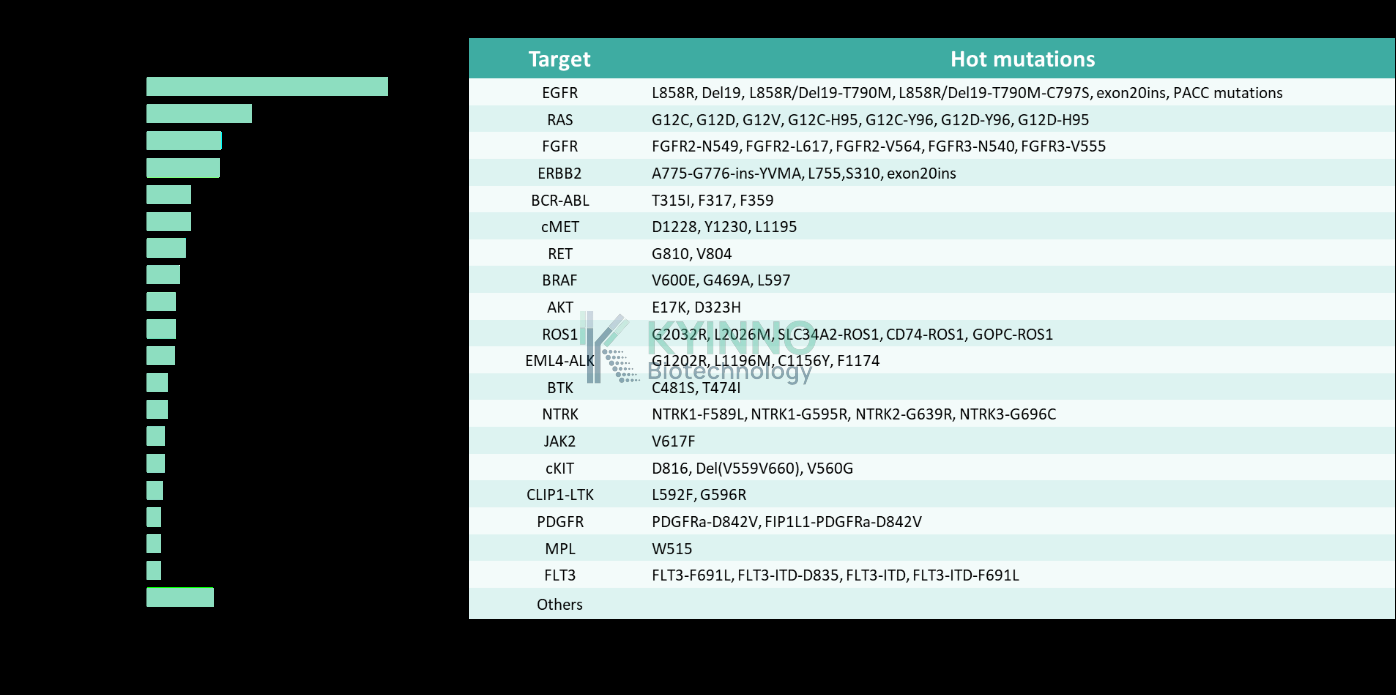
Ba/F3 细胞应用方向
- 激酶转化能力评估
- 激酶下游信号通路研究
- 细胞水平小分子激酶抑制剂高通量筛选
- 细胞水平 PROTAC 高通量筛选
- 动物模型中激酶抑制剂药效评价
- 小分子激酶抑制剂耐药性预测
- 导致小分子激酶抑制剂耐药的突变筛选
Ba/F3 细胞应用案例
1. 筛选导致小分子激酶抑制剂耐药的 EGFR 突变。
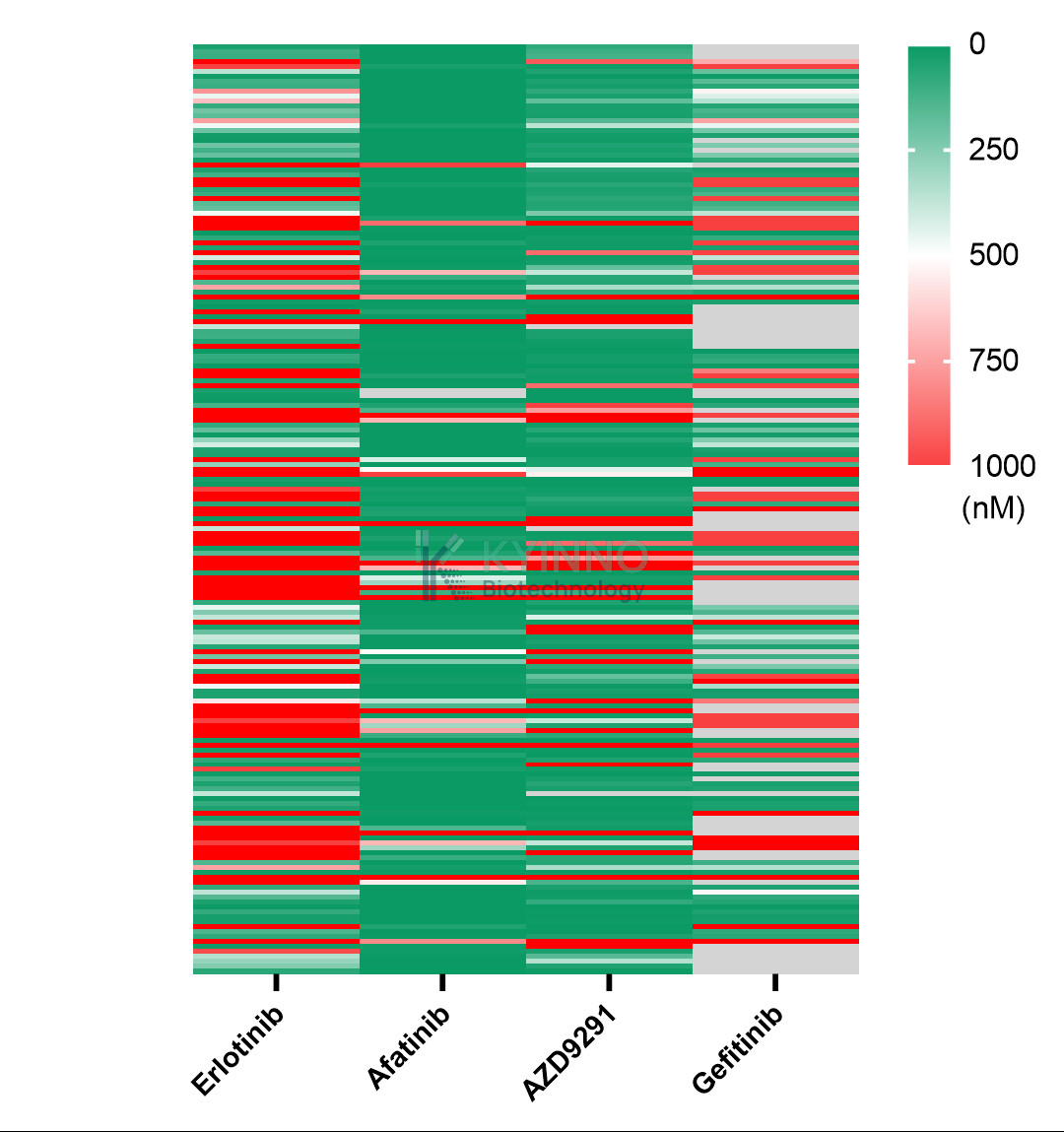
- 图:Ba/F3 EGFR 细胞面板中 EGFR 抑制剂的 IC50。
2. EGFR 抑制剂细胞毒性测试:从体外到体内

- 图:EGFR 抑制剂对体外细胞活力和 EGFR 磷酸化的影响

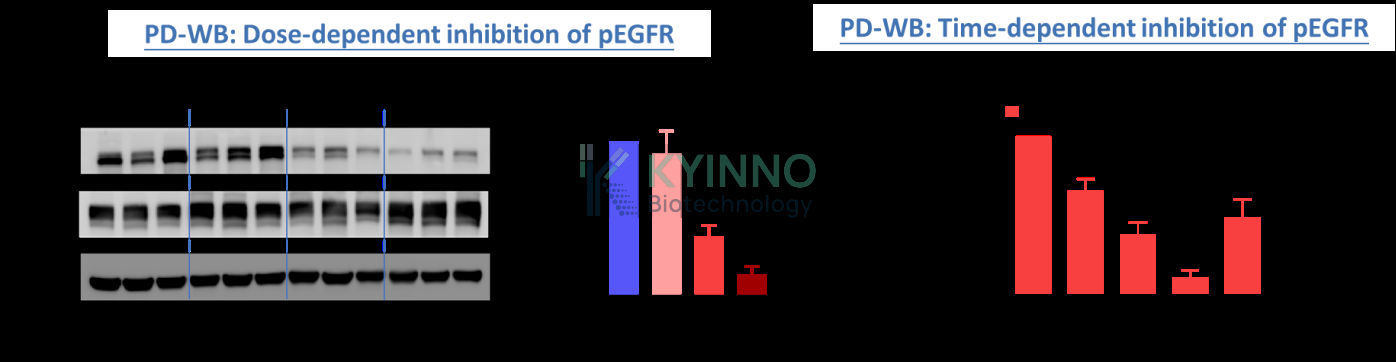
- 图:EGFR 抑制剂的体内药效及 PK/PD 分析。
3. 筛选导致靶向 ETV6-BTK 的小分子激酶抑制剂耐药的突变。
表达 ETV6-BTK 的 Ba/F3 细胞经 ENU 诱导突变后,在无 IL-3 条件下接受 ETV6-BTK 抑制剂伊布替尼处理。该过程产生耐药细胞系,测序结果显示存在 F517L 突变。
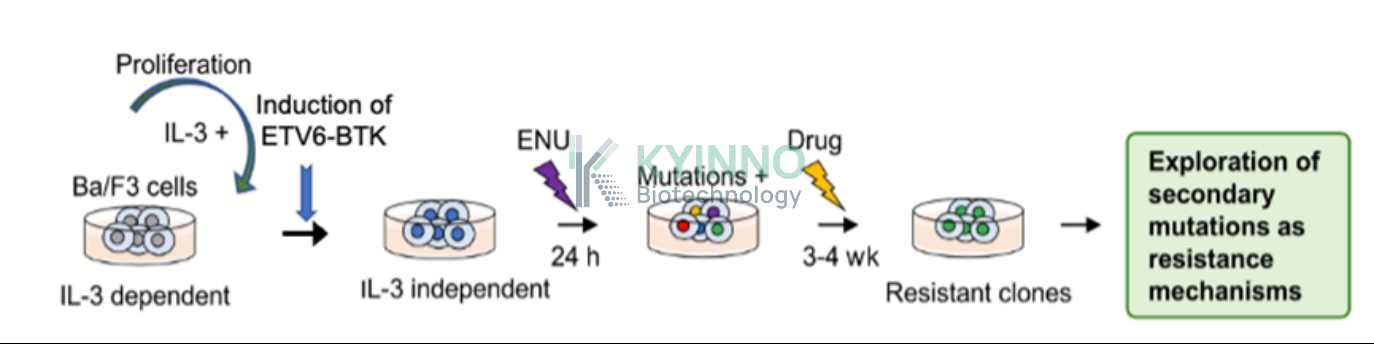

4. 评估 PROTAC 诱导的靶点降解和细胞活力下降
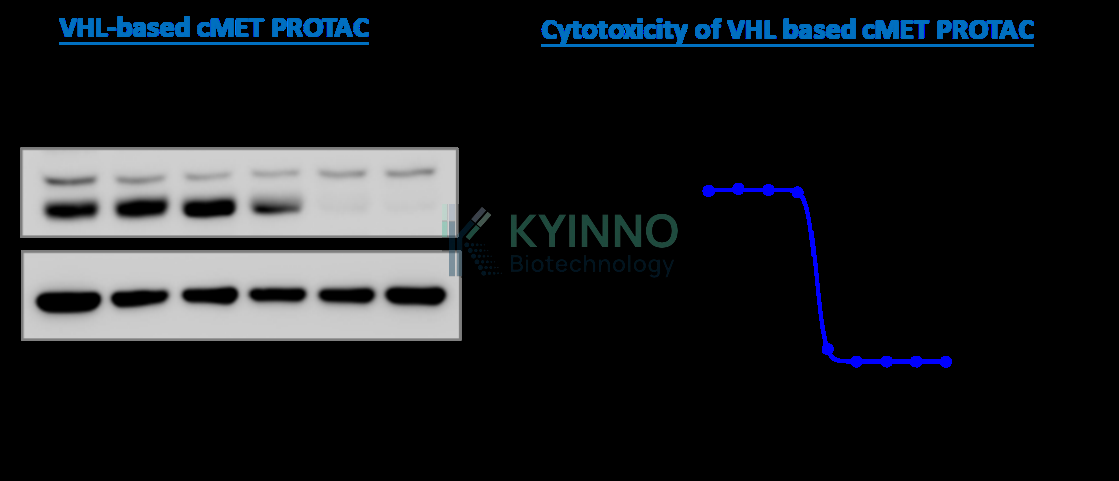
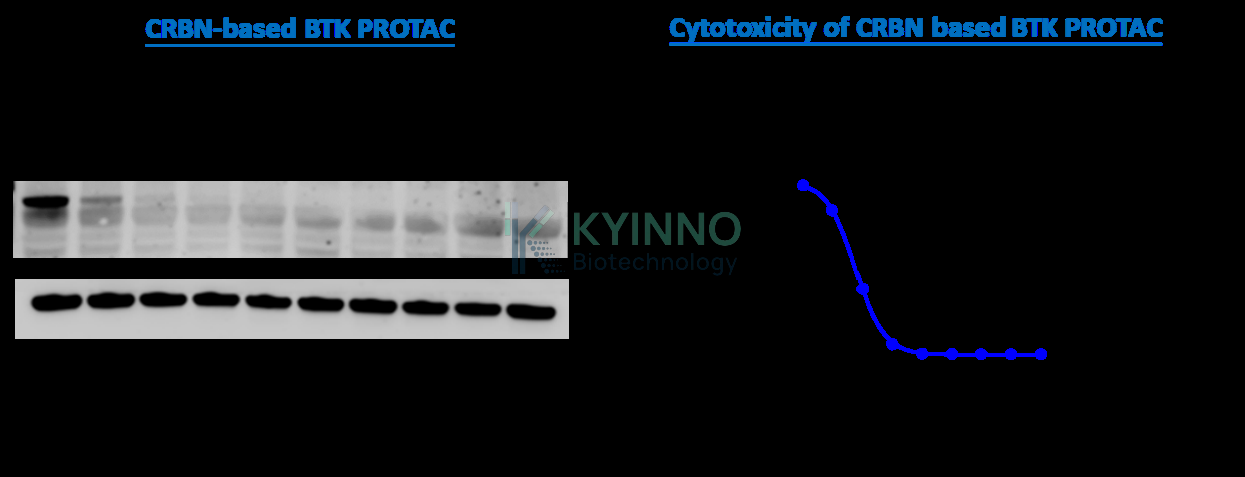
- 图:VHL 型 cMET PROTAC 和 CRBN 型 BTK PROTAC 分别在 Ba/F3 细胞中降解 cMET 和 BTK,并以剂量依赖方式导致细胞毒性。
作为一种多用途细胞工具,Ba/F3 细胞正在突破其在小分子激酶抑制剂评价中的传统角色,越来越多地用于 PROTAC 药物、生长因子类似物和抗体类药物的筛选与评估。凭借多年 Ba/F3 细胞应用经验,Kyinno 已建立覆盖广泛的工程化 Ba/F3 细胞系库,积累了跨多种治疗模式的验证案例,并拥有经验丰富的研究团队。我们可提供从靶点验证到机制研究的一站式综合药物评价解决方案。
参考文献
- Philip Cohen, Darren Cross and Pasi A. Jänne, Kinase drug discovery 20 years after imatinib: progress and future directions. Nature Reviews Drug Discovery 2021; 20:551-569
- Palacios R, Steinmetz M. Il-3-dependent mouse clones that express B-220 surface antigen, contain Ig genes in germ-line configuration, and generate B lymphocytes in vivo. Cell 1985; 41:727-734
- Daley GQ, Baltimore D. Transformation of an interleukin-3 dependent hematopoietic cell line by the chronic myelogenous leukemia-specific p210bcr/abl protein. Proc Nat Acad Sci USA 1988; 85:9312-9316.
- Lacronique V, Boureux A, Valle VD, et al. A TEL-JAK2 fusion protein with constitutive kinase activity in human leukemia. Science1997; 278:1309-1312.
- Mohammad Azam, Robert R. Latek, and George Q. Daley. Mechanisms of Autoinhibition and STI-571/Imatinib Resistance Revealed by Mutagenesis of BCR-ABL. Cell 2003; 112:831-843.
- Takamasa Koga, Kenichi Suda and Tetsuya Mitsudomi. Utility of the Ba/F3 cell system for exploring on-target mechanisms of resistance to targeted therapies for lung cancer. Cancer Science 2022; 113:815-827