基因编辑细胞系
基因编辑细胞系概览
自 2012 年 CRISPR 基因编辑技术问世以来,凭借其操作简便、特异性强和编辑效率高等优势,已成为全球科研人员广泛采用的基因编辑工具。2020 年,CRISPR 系统相关研究成果荣获诺贝尔化学奖。CRISPR 基因编辑技术已被广泛用于探索生物学功能、解析基因信息,并为人类疾病防治和作物设计提供重要策略支持。近年来,CRISPR 技术也持续优化升级,包括降低脱靶效应、拓展编辑位点以及提升递送效率等,将对科学研究、农业和医学领域产生长期而深远的影响。
Kyinno 可提供 200 余种 CRISPR 基因编辑细胞系,涵盖基因敲除和基因敲入细胞,并可根据科研人员的具体需求提供定制化服务。我们的基因编辑细胞系可广泛应用于蛋白或 RNA 生物学功能研究、药物筛选、合成致死研究等多种应用场景。代表性模型包括 CT26-GPC3 等抗原修饰肿瘤细胞系,可用于支持靶点验证和肿瘤免疫学研究。
此外,我们还可结合 pegRNA、Prime Editing 以及脂质纳米颗粒(LNP)递送技术,实现多位点同步编辑,在提升基因编辑效率的同时,最大限度降低脱靶风险。
按产品类型筛选
按分类筛选
按构建方式筛选
按宿主筛选
更多基因编辑细胞系相关产品
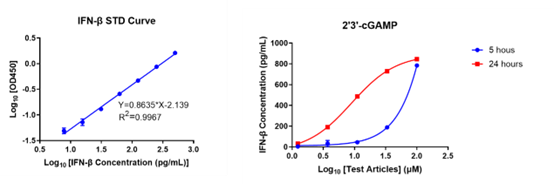
肿瘤及其分泌或释放的多种产物能够重塑肿瘤微环境(TME),从而抑制微环境中免疫细胞的功能。康源博创拥有多种免疫分子细胞系资源,覆盖 PD-1、IL-2RB、IL-6 等免疫相关分子,可为肿瘤免疫机制研究、靶点验证及药物评价提供支持。

自 2012 年 CRISPR 基因编辑技术出现以来,其因简便、高特异性和高效率等特点,迅速成为全球科学家首选的基因编辑工具之一。2020 年,CRISPR 技术相关研究成果荣获诺贝尔化学奖,进一步彰显了其在生命科学和药物研发领域的重要价值。
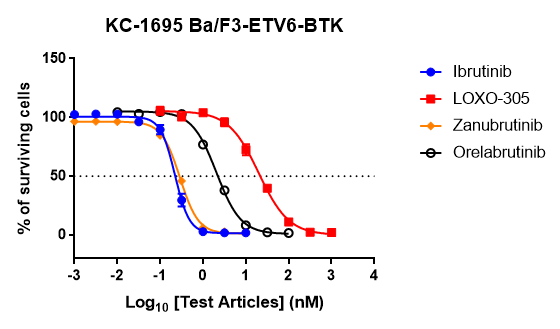
激酶广泛参与细胞代谢、信号转导和物质转运等关键细胞过程,在人体生理调控中具有重要作用。康源博创拥有 850 余种 Ba/F3 及人源激酶细胞系资源,覆盖多条重要信号通路,可为靶点验证和药物筛选研究提供支持。
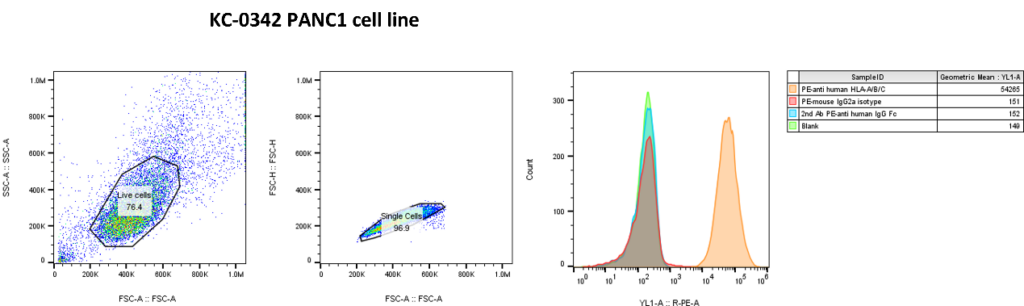
康源博创拥有丰富的肿瘤抗原细胞系资源,覆盖 EGFR、VEGFR、FGFR、ERBB2、HLA、GPRC5D、ROR1、CLDN18.2、GPC3、Siglec-15、DLL3、LAG-3、B7-H3、B7-H4、B7-H6、FAP 等多种肿瘤相关靶点,可为肿瘤免疫研究、靶点验证及抗肿瘤药物评价提供支持。